Cos’e la retinopatia diabetica e l’edema maculare diabetico
Il diabete è attualmente considerato un drammatico problema di salute pubblica, legato ad un progressivo incremento di fattori di rischio come lo stile di vita sedentario, l’urbanizzazione, l’aumento dell’età media e dell’obesità. Ad oggi la retinopatia diabetica (RD), complicanza oculare del diabete, è una delle principali cause di perdita visiva in età lavorativa nei paesi industrializzati. La prevalenza della retinopatia diabetica è maggiore nei diabetici di tipo 1 rispetto al tipo 2 e varia in relazione alla durata del diabete, al controllo glicometabolico, alla pressione arteriosa e al livello ematico di colesterolo e lipidi.
La retinopatia diabetica origina da un’alterazione del microcircolo secondaria al danno cronico derivante dall’iperglicemia. Si divide principalmente in due forme: quella non proliferante (meno grave) e quella proliferante (più invalidante).
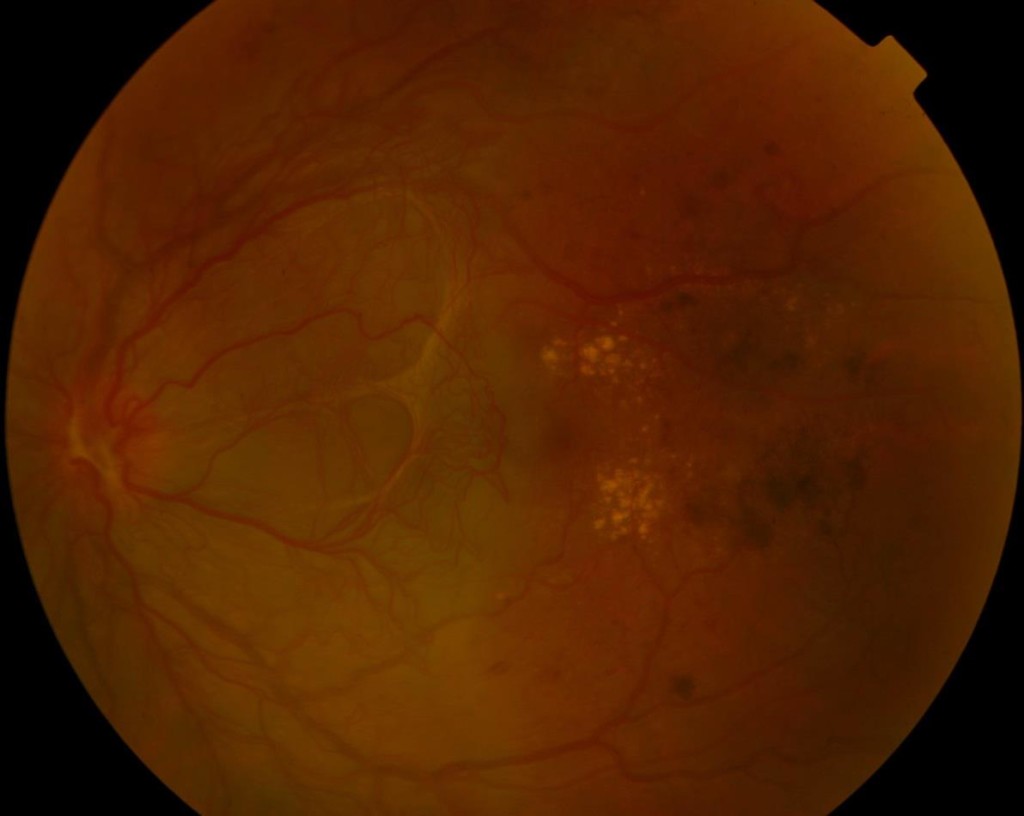
Nella retinopatia diabetica non proliferante sono identificabili diversi tipi di lesioni, fra cui i microaneurismi (dilatazioni terminali di piccoli vasi sanguigni), le emorragie retiniche, gli essudati duri (materiale lipidico che trasuda dai vasi retinici con alterata permeabilità e si accumula nello spessore della retina) e i noduli cotonosi (aree di infarto delle fibre nervose retiniche).
Nella retinopatia diabetica proliferante, a seguito di uno stimolo ischemico (con conseguente mancata ossigenazione della retina), si apprezza la crescita di nuovi vasi sanguigni patologici (neovasi). Tali neovasi sono caratterizzati da una struttura anomala, più fragile, che ne predispone alla rottura, determinando un versamento emorragico in cavità vitrea (emovitreo) e portando così ad una invalidante perdita della vista. Nella forma proliferante di RD si possono sviluppare aderenze patologiche tra la retina e il vitreo, gel antistante, con trazioni sulla retina stessa e rischio di distacco di retina di tipo trazionale.
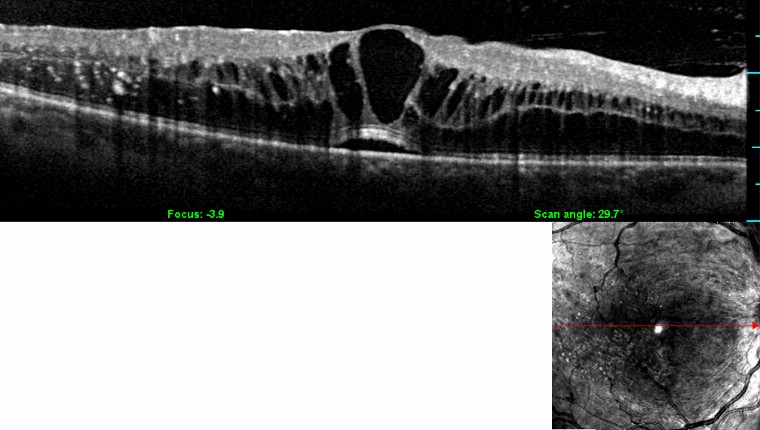
Un’altra delle complicanze oculari temibili della retinopatia diabetica è la formazione dell’edema maculare diabetico (EMD), che può insorgere sia nella forma proliferante che in quella non proliferante. L’EMD è causato dalla raccolta di liquido nella regione centrale (la macula, sede della visione distinta) determinata dalla permeabilità aumentata dei piccoli vasi.
Sintomi
Sebbene negli stadi precoci, la retinopatia diabetica sia spesso asintomatica, la comparsa dell’EMD si associa tipicamente alla comparsa di alcuni sintomi caratteristici, fra cui l’offuscamento visivo e la presenza di visione deformata (metamorfopsie). Tali alterazioni comportano tipicamente difficoltà nello svolgimento delle attività quotidiane che richiedono la visione distinta, fra cui la lettura e la guida e, in certi casi, compromettono la capacità lavorativa dell’individuo.
La comparsa invece di sanguinamenti e emovitrei in corso di retinopatia diabetica proliferante si associa a un calo improvviso e talora importante della funzione visiva che inducono il paziente a una valutazione oculistica immediata.
Diagnosi
L’oculista, mediante l’esame del fondo oculare con la pupilla dilatata, è in grado di diagnosticare i segni di RD negli stadi iniziali prima dell’insorgenza dei sintomi. Per questo motivo i pazienti affetti da diabete dovrebbero sottoporsi periodicamente all’esame del fondo oculare, anche in assenza di una sintomatologia specifica, in modo da poter identificare precocemente la comparsa di lesioni prima dello sviluppo di ulteriori complicanze, al fine di correggere lo stile di vita o effettuare terapie specialistiche.
In caso di identificazione di EMD, l’oculista potrà richiedere alcuni esami più approfonditi fra cui la fluorangiografia retinica e la tomografia retinica a coerenza ottica (OCT). Con la fluorangiografia è possibile apprezzare le aree di alterata permeabilità vascolare che predispongono alla formazione dell’edema maculare e identificare inoltre le zone di ischemia retinica periferica e la comparsa di neovasi, che insorgono in caso di retinopatia diabetica proliferante. Con l‘esame OCT è possibile apprezzare la formazione di EMD e di monitorarne nel tempo la progressione, dopo eventuale terapia.
Terapia
Prevenzione
Un adeguato controllo del diabete, associato ad un mantenimento del corretto profilo pressorio e lipidico è indispensabile per prevenire l’insorgenza della retinopatia e dell’edema maculare.
Trattamento laser
Il trattamento laser fotocoagulativo, introdotto negli anni ’80, è stato considerato per decenni l’unica terapia validata sia in corso di EMD, sia in corso di RD proliferante. Nel caso di EMD, le due modalità di trattamento utilizzate prevedono ancora oggi la tipologia “focale” e lo schema a “griglia”.
Nel trattamento focale, alcuni spot laser vengono indirizzati su un’area localizzata della retina, con lo scopo di occludere i microaneurismi e le sedi di alterata permeabilità vascolare.
Nel trattamento a griglia, multipli spot laser vengono applicati secondo uno schema predefinito, per trattare un’area più vasta di edema retinico.
Il trattamento laser si è dimostrato efficace e sicuro nel trattamento dell’edema maculare, anche se non è scevro da effetti collaterali, fra cui la comparsa di alcune cicatrici retiniche, che possono determinare alterazioni del campo visivo. Per questo motivo negli anni sono state sviluppate tecniche alternative di trattamento laser, meno invasive, con minore intensità e impatto sulla retina. Queste nuove strategie laser, di tipo leggero o modificato, hanno dimostrato comunque risultati favorevoli. Il laser “sottosoglia” è un nuovo promettente tipo di laser, non invasivo, con effetto non visibile, la cui validità è oggetto di ricerche scientifiche. Inoltre recentemente sono state introdotte nuove strumentazioni laser che utilizzano schemi semiautomatici di trattamento con tecnologie ad alta precisione in grado di applicare gli spot laser in maniera meno dolorosa e più accurata.
Nel caso di RD proliferante il trattamento laser rimane lo strumento fondamentale per la distruzione delle aree retiniche ischemiche evidenziate con l’esame della fluorangiografia; tale ablazione fotocoagulativa delle aree retiniche non ossigenate comporta la regressione dei neovasi presenti, la prevenzione della comparsa di ulteriori neovascolarizzazioni e di tutte le complicanze associate alla loro presenza.
Iniezioni intravitreali
Mediante l’iniezione intraoculare (intravitreale) è possibile rilasciare direttamente in cavità vitrea alcuni farmaci in modo da massimizzarne l’effetto terapeutico oculare, riducendo i rischi legati alla somministrazione sistemica.
Ad oggi le tecniche iniettive intravitreali permettono di rilasciare due classi molecole: farmaci steroidei e molecole in grado di inibire il fattore di crescita endoteliale vascolare (famaci anti-VEGF), una sostanza implicata nella formazione dell’EMD e della RD proliferante.
Se finora con l’utilizzo del laser era possibile solamente ottenere una stabilizzazione dell’acuità visiva (in modo da prevenire ulteriori peggioramenti della visione), ora con le iniezioni intravitreali è possibile favorire un miglioramento della funzione visiva compromessa dalla malattia. Pur essendo una tecnica ben tollerata, sono descritti in rari casi eventi avversi legati alla procedura meccanica iniettiva, fra cui l’endoftalmite (infezione del bulbo oculare), l’emovitreo, il distacco del corpo vitreo, la formazione di rotture retiniche e il distacco di retina.
Steroidi intravitreali
Gli steroidi sono utilizzati nel trattamento dell’EMD per le loro proprietà anti-infiammatorie e anti-edemigene. Tuttavia possono essere associati ad un rischio di sviluppare il glaucoma (patologia caratterizzata dall’aumento della pressione intraoculare) e determinare l’insorgenza o la progressione della cataratta.
L’impianto di desametazone a lento rilascio (Ozurdex®, Allergan Inc.) è stato recentemente validato anche nel trattamento dell’EMD. Si tratta di una dispositivo biodegradabile di desametazone, privo di conservanti, che viene rilasciato in cavità vitrea mediante un applicatore monouso. L’impianto si è dimostrato sicuro ed efficace nel trattamento dell’EMD, rivelando una durata dell’effetto terapeutico variabile da 4 a 6 mesi circa.
Altri dispositivi di steroidi a rilascio prolungato –fluocinolone acetonide- non biodegradabili (Iluvien® Alimera Sciences, Alpharetta, GA) hanno dimostrato un’efficacia in termini di recupero dell’acuità visiva e una lunga durata d’azione (30 o più mesi), ma associata ad un tasso significativo di effetti collaterali. L’utilizzo di tali impianti può essere consigliato in caso in pazienti affetti da EMD persistente, già operati di cataratta.
Iniezioni intravitreali di farmaci Anti-VEGF
I farmaci attualmente disponibili in grado di inibire il fattore di crescita endoteliale vascolare sono il ranibizumab, l’aflibercept e il bevacizumab. Questa classe di molecole si è dimostrata efficace in numerose patologie retiniche e nell’EMD, pur avendo come grosso limite la ridotta durata dell’effetto terapeutico (variabile da 1 a 2 mesi circa). Pur essendo una tecnica relativamente sicura, si segnalano possibili eventi avversi locali secondari alla frequente ripetizione dell’iniezione intravitreale e eventi avversi di carattere generale legati all’inibizione sistemica del VEGF, fra cui l’esposizione ad accidenti cardiovascolari fatali e non fatali o a sanguinamenti gastro-intestinali. Inoltre esiste la possibilità di ridurre la compliance del paziente alla cronicità del trattamento.
Il ranibizumab (Lucentis®, Genentech, Inc., South San Francisco, CA) è approvato per il trattamento dell’EMD, della degenerazione maculare senile, della degenerazione maculare miopica e dell’edema maculare in corso di occlusione venosa retinica. Numerosi studi clinici randomizzati hanno dimostrato l’efficacia e la sicurezza dal ranibizumab da solo o in aggiunta al trattamento laser o alla chirurgia, dopo confronto con il placebo o con il trattamento laser stesso. I risultati hanno dimostrato che le iniezioni intravitreali di ranibizumab combinate al laser (immediato o posticipato) erano più efficaci del solo trattamento laser (e placebo); inoltre la fotocoagulazione laser applicata immediatamente dopo la terapia iniettiva ha dato risultati peggiori rispetto alla sua posticipazione a 24 o più settimane.
L’aflibercept (Eylea®, noto nella letteratura scientifica come VEGF Trap-Eye, Regeneron Inc., New York; Bayer HealthCare Pharmaceuticals, Berlino, Germania) è in grado di bloccare non solo il VEGF-A ma anche il fattore di crescita placentare ed è stato recentemente approvato dalla Commissione Europea per il trattamento dell’EMD. La nuova indicazione si affianca alle precedenti già approvate per il trattamento della degenerazione maculare senile e dell’edema maculare in corso di occlusione venosa. In due trials di fase 3 (gli studi VISTA e VIVID), l’aflibercept (2mg) somministrato mensilmente e l’aflibercept (2mg) iniettato ogni 8 settimane dopo le prime 5 dosi mensili è risultato più efficace del solo trattamento laser .
Il bevacizumab (Avastin®, Genentech In. San Francisco, CA, USA) è approvato solo per il trattamento dei tumori in fase metastatica. Tuttavia il bevacizumab intravitreale è stato ed è utilizzato secondo modalità off-label (senza approvazione della FDA o dell’EMA) ma sulla base di numerosi studi clinici, dimostrando un effetto terapeutico, nel trattamento di numerose malattie retiniche, fra cui l’EMD, la degenerazione maculare senile e l’edema maculare in corso di occlusione venosa. L’efficacia delle iniezioni intravitreali di bevacizumab, a differenti dosaggi (1,25mg e 2,5mg), è stata oggetto di diversi studi nel trattamento dell’EMD e risultato efficace.
Vitrectomia via pars-plana
Il vitreo gioca un ruolo importante nella formazione di anomalie dell’interfaccia vitreoretinica, cioè di aderenze patologiche fra il vitreo stesso e la retina, fra cui la membrana epiretinica e la trazione vitreomaculare. Nel primo caso si tratta di una pellicola (cellophane maculare) che in seguito ad aggravamento e contrazione, può provocare ispessimento e deformazione del profilo retinico centrale. Nel secondo caso esiste una adesione patologica con trazione fra vitreo e retina, talmente tenace da portare ad un sollevamento della regione maculare. In questi casi di edema maculare trazionale, la chirurgia vitreoretinica trova la propria indicazione terapeutica. L’intervento prevede l’asportazione del corpo vitreo, mediante inserimento di una sonda (vitrectomo) che frammenta e aspira la gelatina vitreale. Successivamente vengono asportate delicatamente le aderenze vitreoretiniche responsabili della formazione dell’EMD e, nel caso di retinopatia diabetica proliferante, vengono tagliate le membrane fibrovascolari che determino trazione o distacchi retinici. Inoltre è possibile asportare anche la membrana limitante interna, lo strato più interno della retina, che agisce da impalcatura responsabile della recidiva di membrana epiretinica (procedura chiamata peeling della membrana limitante interna).
Vitreolisi enzimatica
La vitreolisi enzimatica è una nuova possibilità terapeutica in caso di trazione vitreo-maculare. Consiste nell’iniezione in camera vitrea di enzimi (fra cui plasmina, ialuronidasi, condroitinasi, dispasi) in grado di indurre la separazione del corpo vitreo dalla retina (distacco del corpo vitreo) e la successiva risoluzione della trazione vitreo-maculare. Attualmente l’iniezione di ocriplasmina (Jetrea®, Alcon) è indicata nei pazienti adulti affetti da trazione vitreo maculare a da foro maculare del diametro inferiore o pari a 400μ.
Conclusioni
La gestione dell’EMD e della retinopatia diabetica in generale è cambiata enormemente negli ultimi anni. Se fino a poco tempo fa il laser era considerato l’unica possibilità terapeutica, ad oggi esistono nuovi validati trattamenti in grado non solo di evitare il deterioramento visivo ma anche di promuovere un miglioramento della capacità visiva. Ad oggi lo specialista può contare, oltre che sul trattamento laser e sulla chirurgia in casi selezionati, su un discreto numero di opzioni terapeutiche e di differenti farmaci con dimostrata efficacia. Per questo motivo, recenti algoritmi terapeutici e nuove linee guida sono state pubblicate in modo da guidare lo specialista verso una gestione individualizzata della malattia e in modo da ottenere il miglior risultato visivo .
Il compenso glicometabolico e la compliance del paziente nel seguire controlli e terapie ripetuti nel tempo sono fondamentali al fine di ottenere e mantenere i migliori risultati anatomici e funzionali. La gestione delle complicanze della retinopatia diabetica implica un impegno crescente di risorse e la necessità di strutture dedicate per far fronte al numero drammaticamente in aumento di pazienti affetti da diabete mellito e dalle sue complicanze.
Bibliografia
- Shaw JE, Sicree RA, Zimmet PZ. Global estimates of the prevalence of diabetes for 2010 and 2030. Diabetes Res Clin Pract 2010;87:4-14
- Yau JW, Rogers SL, Kawasaki R et al. Global prevalence and major risk factors of diabetic retinopathy. Diabetes Care 2012;35:556-64
- Early Treatment Diabetic Retinopathy Study Research Group. Photocoagulation for diabetic macular edema, ETDRS report no 1. Arch Ophthalmol 1985;103:1796–1806
- Early Treatment Diabetic Retinopathy Study Research Group. Treatment techniques and clinical guidelines for photocoagulation of diabetic macular edema. Early Treatment Diabetic Retinopathy Study report number 2. Ophthalmology 1987;94:761–764
- Early Treatment Diabetic Retinopathy Study Research Group. Techniques for scatter and local photocoagulation treatment of diabetic retinopathy. ETDRS report number 3. Int Ophthalmol Clin 1987;27:254–264
- Early Treatment Diabetic Retinopathy Study Research Group. Photocoagulation for diabetic macular edema. ETDRS report number 4. Int Ophthalmol Clin 1987;27:265–272
- Bandello F, Polito A, Borrello MD et al. ‘Light’ versus ‘classic’ laser treatment for clinically significant diabetic macular oedema. Br J Ophthalmol 2005;89:864–870
- Desmettre TJ, Mordon SR, Buzawa DM et al. Micropulse and continuous wave diode retinal photocoagulation: visible and subvisible lesion parameters. Br J Ophthalmol 2006;90:709–712
- Kumar V, Ghosh B, Mehta DK et al. Functional outcome of subthreshold versus threshold diode laser photocoagulation in diabetic macular oedema. Eye 2010;24:1459–1465
- Blumenkranz MS, Yellachich D, Andersen DE et al. Semiautomated patterned scanning laser for retinal photocoagulation. Retina 2006:26:370–376
- Kozak I, Oster SF, Cortes MA et al. Clinical evaluation and treatment accuracy in diabetic macular edema using navigated laser photocoagulator NAVILAS. Ophthalmology 2011;118:1119–1124
- Kernt M, Cheuteu RE, Cserhati S et al. Pain and accuracy of focal laser treatment for diabetic macular edema using a retinal navigated laser (Navilas). Clin Ophthalmol 2012;6:289–296
- Boyer DS, Yoon YH, Belfort R Jr et al; Ozurdex MEAD Study Group. Three-Year, Randomized, Sham-Controlled Trial of Dexamethasone Intravitreal Implant in Patients with Diabetic Macular Edema. Ophthalmology 2014;121:1904-14
- Pearson PA, Comstock TL, Ip M et al. Fluocinolone acetonide intravitreal implant for diabetic macular edema: a 3-year multicenter, randomized, controlled clinical trial. Ophthalmology 2011;118:1580–1587
- Schmidt-Erfurth U, Lange GE, Holz FG et al. Three-year outcomes of individualized ranibizumab treatment in patients with diabetic macular edema: the RESTORE extension study. Ophthalmology 2014;121:1045-53
- Diabetic Retinopathy Clinical Research Network; Elman MJ, Ayala A, Bressler Qin H et al. Intravitreal ranibizumab for diabetic macular edema with prompt versus deferred laser treatment: three-year randomized trial results. Ophthalmology 2012;119:2312–2318
- Korobelnik JF, Do DV, Schmidt-Erfurth U et al. Intravitreal aflibercept for diabetic macular edema. Ophthalmology 2014;121(11):2247-54.
- Rajendram R, Fraser-Bell S, Kaines A et al. A 2-year prospective randomized controlled trial of Intravitreal Bevacizumab or Laser Therapy (BOLT) in the management of diabetic macular edema: 24-month data: report 3. Arch Ophthalmol 2012;130:972–979
- Diabetic Retinopathy Clinical Research Network Writing Committee; Haller JA, Qin H, Apte RS et al. Vitrectomy outcomes in eyes with diabetic macular edema and vitreomacular traction. Ophthalmology 2010;117:1087–1093.e3
- Bandello F, Zucchiatti I, Lattanzio R et al. Diabetic Macular Edema. In: Bandello F, Zarbin M, Lattanzio R et al, editors. Clinical Strategies in the Management of Diabetic Retinopathy. Springer-Verlag, Berlin Heidelberg, 2014;104-107
- Bandello F, Cunha-Vaz J, Chong NV et al. New approaches for the treatment of diabetic macular oedema: recommendations by an expert panel. Eye (Lond) 2012;26:485–493
- Mitchell P, Wong TY; Diabetic Macular Edema Treatment Guideline Working Group. Management paradigms for diabetic macular edema. Am J Ophthalmol 2014;157:505-13.e1-8